
炎症小体是多蛋白复合物,其活性与生理性和病理性炎症密切相关。炎症小体激活的标志性事件为细胞因子白细胞介素-1β(IL-1β)和白细胞介素-18(IL-18)的成熟,以及gasdermin D蛋白的加工——该过程介导固有免疫系统细胞的细胞因子释放和焦亡。
炎症小体是一类高分子量复合物,可激活炎性半胱天冬酶(caspase)和白细胞介素-1家族细胞因子(IL-1β、IL-18,受刺激不同还可能包括IL-1α)。目前已发现多种炎症小体,其包含的传感器蛋白各有不同,如NLRP1(NALP1)、NLRP3(NALP3)、IPAF(NLRC4)、NLRP6(NALP6)、NLRP10(NALP10)、NLRP12(NALP12)、Pyrin蛋白、维甲酸诱导基因I(RIG-I)和黑色素瘤缺失蛋白2(AIM-2)。这类炎症小体大多需要衔接蛋白Asc(含半胱天冬酶募集结构域的凋亡相关斑点样蛋白)将半胱天冬酶-1募集至炎症小体复合物中。半胱天冬酶-1与炎症小体结合后发生切割并激活,进而切割其多种靶蛋白,促使促炎性细胞因子IL-1β成熟并分泌。
炎症小体可通过多种信号激活,包括活菌、微生物毒素、异源化合物、颗粒物质、细胞质中的病原体相关分子模式(PAMPs)和/或内源性损伤相关分子模式(DAMPs)。相关细节可参考我司的NLRP3炎症小体挂图。炎症小体的活性与多种炎症反应的诱导存在因果关系,这些反应对机体既可能有益,也可能有害。
有益的炎症反应可维持组织的稳态功能(如创伤或病原体入侵后检测并修复组织损伤);有害的炎症反应则包括颗粒诱导的无菌性炎症——如尿酸单钠(MSU)结晶等宿主来源颗粒引发的炎症(与痛风发病机制相关),以及石棉、二氧化硅、金属纳米颗粒等环境和工业颗粒经吸入后诱导的肺部炎症。
越来越多的证据表明,炎症小体的活性还与多种其他疾病相关,包括癌症、代谢性疾病(如2型糖尿病、动脉粥样硬化)、部分神经退行性疾病(如阿尔茨海默病、朊病毒病、帕金森病)、自身免疫性疾病(如多发性硬化症)和炎症性肠病。此外,炎症小体还能提升疫苗效力,对宿主发挥有益作用。
1. NLRP3炎症小体的激活与调控,J. Xu & G. Nunez,《生物化学与生物物理进展》,2023年,第48卷,331页
2. 定位与细胞信号的协同作用如何激活NLRP3炎症小体,A. Akbal等,《细胞与分子免疫学杂志》,2022年,第19卷,1201页
3. 炎性半胱天冬酶:炎症小体激活半胱天冬酶的统一模型,C. Ross等,《免疫学年度综述》,2022年,第40卷,249页
抗NLRP3/NALP3单克隆抗体(Cryo-2),货号AG-20B-0014-C100,规格100微克
克隆号 | Cryo-2 |
同型 | 小鼠IgG2b |
免疫原 | 重组小鼠NLRP3/NALP3(吡喃结构域/1-93位氨基酸) |
应用 | 免疫细胞化学(ICC)、免疫组化(IHC)、免疫沉淀(IP)、蛋白质免疫印迹(WB,工作浓度1微克/毫升),详见在线实验方案 |
特异性 | 识别人和小鼠的NLRP3/NALP3 |
引用量超1000次! |
|
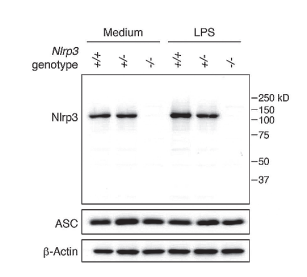
实验图:采用NLRP3单克隆抗体(Cryo-2,货号AG-20B-0014-C100)在小鼠巨噬细胞中检测到小鼠NLRP3蛋白。
半胱天冬酶-1检测、标准及其他抗体、预激活与激活、NLRP3抑制剂/激活剂、代谢调控、微管组装、炎症小体/焦亡、Gasdermin D与E、鞭毛蛋白与NLRC4、研究进展
●蛋白质免疫印迹(WB)检测活化的小鼠p10和p20型半胱天冬酶-1
1.抗小鼠半胱天冬酶-1(p10)单克隆抗体(Casper-2),货号AG-20B-0044-C100(100微克)、AG-20B-0044B-C100(生物素标记,100微克)
克隆号 | Casper-2 |
同型 | 小鼠IgG2a |
免疫原 | 重组小鼠半胱天冬酶-1 |
应用 | 蛋白质免疫印迹(WB,工作浓度1微克/毫升),详见在线实验方案 |
特异性 | 识别小鼠内源性全长及活化的半胱天冬酶-1(p10片段) |
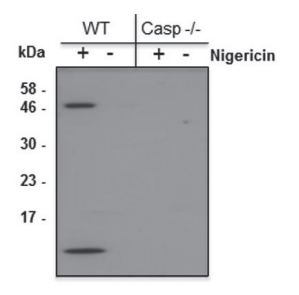
实验图:采用抗小鼠半胱天冬酶-1(p10)单克隆抗体(Casper-2,货号AG-20B-0044),通过免疫印迹在经5微摩尔尼日利亚菌素(货号AG-CN2-0020)处理30分钟的野生型和半胱天冬酶-1基因敲除小鼠的分化骨髓源树突状细胞(BMDCs)上清液中检测到小鼠半胱天冬酶-1(p10)。
2.抗小鼠半胱天冬酶-1(p20)单克隆抗体(Casper-1),货号AG-20B-0042-C100(100微克)、AG-20B-0042B-C100(生物素标记,100微克)
克隆号 | Casper-1 |
同型 | 小鼠IgG1 |
免疫原 | 重组小鼠半胱天冬酶-1 |
应用 | 蛋白质免疫印迹(WB,1微克/毫升)、免疫组化(IHC,石蜡切片)、免疫沉淀(IP),详见在线实验方案 |
特异性 | 识别小鼠内源性全长及活化的半胱天冬酶-1(p20片段) |
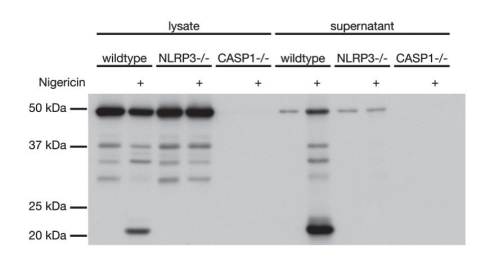
实验图:采用抗小鼠半胱天冬酶-1(p20)单克隆抗体(Casper-1,货号AG-20B-0042),通过免疫印迹在野生型、NLRP3基因敲除和半胱天冬酶-1基因敲除小鼠的分化骨髓源树突状细胞(BMDCs)的细胞提取物和上清液中检测到小鼠半胱天冬酶-1(p20)。
3.抗人半胱天冬酶-1(p20)单克隆抗体(Bally-1),货号AG-20B-0048-C100(100微克)、AG-20B-0048B-C100(生物素标记,100微克)
克隆号 | Bally-1 |
同型 | 小鼠IgG1 |
免疫原 | 重组人半胱天冬酶-1 |
应用 | 蛋白质免疫印迹(WB,1微克/毫升),详见在线实验方案 |
特异性 | 识别人内源性全长及活化的半胱天冬酶-1(p20片段) |

实验图:采用抗人半胱天冬酶-1(p20)单克隆抗体(Bally-1,货号AG-20B-0048),通过免疫印迹检测到人半胱天冬酶-1(p20)。
实验方法:用0.5微摩尔佛波酯(PMA,货号AG-CN2-0010)诱导THP1细胞分化3小时,经5微摩尔尼日利亚菌素处理1小时(激活组,泳道2)或不处理(未激活组,泳道1)后,取上清液通过蛋白质免疫印迹分析半胱天冬酶-1。取30微升上清液经还原条件下的十二烷基-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离,转印至硝酸纤维素膜,与1微克/毫升的抗人半胱天冬酶-1(p20)单克隆抗体(Bally-1)孵育,采用化学发光检测系统显色。
一种替代蛋白质免疫印迹的定量检测方法,可检测炎症小体激活引发的半胱天冬酶-1切割与分泌。
1. 小鼠半胱天冬酶-1配对检测试剂盒,货号AG-46B-0003-KI01,规格5块96孔板
○ 特异性:检测小鼠半胱天冬酶-1(p10和p20结构域)
○ 种属反应性:小鼠
○ 灵敏度:100皮克/毫升
○ 检测范围:0.15纳克/毫升~10纳克/毫升
○ 检测类型:比色法/夹心ELISA
○ 样本类型:细胞培养上清液
2. 小鼠半胱天冬酶-1酶联免疫吸附测定(ELISA)试剂盒,货号AG-45B-0002-KI01,规格96孔
○ 特异性:检测小鼠半胱天冬酶-1(p10和p20结构域)
○ 种属反应性:小鼠
○ 灵敏度:33皮克/毫升
○ 检测范围:15皮克/毫升~1000皮克/毫升
○ 检测类型:比色法/夹心ELISA
○ 样本类型:细胞培养上清液、血清、血浆
实验技术缩写:FACS=流式细胞术;FUNC=功能学应用;ICC=免疫细胞化学;IHC=免疫组化;IP=免疫沉淀;WB=蛋白质免疫印迹
配方缩写:PF=无防腐剂
种属缩写:Hu=人;Ms=小鼠;Rt=大鼠;Rb=兔;Prm=灵长类
抗Asc多克隆抗体(AL177),货号AG-25B-0006-C100(100微克)、AG-25B-0006PF-C100(无防腐剂,100微克)、AG-25B-0006TS-C100(ATTO 647N标记,100微克)
• 来源:兔
• 免疫原:人Asc蛋白N端对应氨基酸合成肽
• 应用:ICC、IHC(石蜡切片)、IP、WB、功能学应用(抑制)*
• 特异性:识别人和小鼠的Asc蛋白
*可抑制Asc与NLRP3的相互作用,从而在细胞提取物中阻断半胱天冬酶-1的加工。
Asc抗体(AL177)封闭肽,货号AG-37B-0001-C100,规格100微克;
Asc(AL177)抗体+封闭肽套装,货号AG-44B-2000-KI01,规格1套。
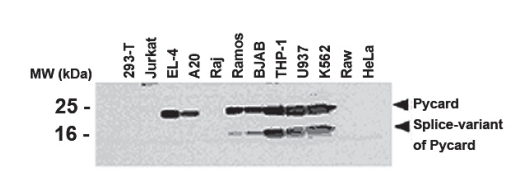
实验图:采用抗Asc多克隆抗体(AL177,货号AG-25B-0006)对人和小鼠细胞系进行蛋白质免疫印迹分析。提取多种人细胞系(293-T、Jurkat、Raj、Ramos、BJAB、THP-1、U937、K562、Raw、HeLa)和小鼠细胞系(EL-4、A20)的总蛋白,经SDS-PAGE分离后,用1:1000稀释的抗Asc多克隆抗体(AL177)检测Pycard蛋白,用1:5000稀释的辣根过氧化物酶偶联抗兔IgG抗体进行化学发光(ECL)检测。
分子量(道尔顿):25kDa-Pycard;16kDa-Pycard剪接变体。
抗小鼠NLRP1b单克隆抗体(2A12),货号AG-20B-0084-C100,规格100微克,应用:WB。
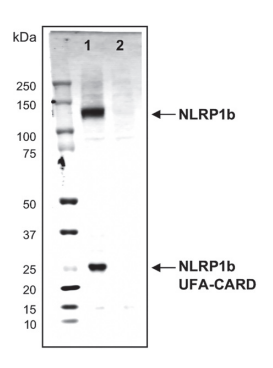
实验图:采用NLRP1b单克隆抗体(2A12,货号AG-20B-0084),在小鼠Raw264.7细胞(泳道1)和NLRP1b基因敲除的Raw264.7细胞(泳道2)的细胞提取物(约30微克)中检测到小鼠NLRP1b(全长和UFA-CARD片段)。
相关文献:功能性降解:病原体多种酶激活NLRP1炎症小体的机制,A. Sandstrom等,《科学》,2019年,第364卷,eaau1330。
抗ZBP1单克隆抗体(Zippy-1),货号AG-20B-0010-C100,规格100微克,应用:ICC、IP、WB。
双链RNA结合蛋白ZBP1是干扰素生物学中的关键因子,参与病毒感染和炎症调控,可激活NLRP3炎症小体、干扰素通路,以及由PANoptosome复合物调控的多种程序性细胞死亡。近期研究表明,RNA编辑酶ADAR1可抑制ZBP1的激活。
1. 检测细菌感染诱导的炎症小体激活,P. Broz & D.M. Monack,《分子生物学方法》,2013年,第1040卷,65页
2. 检测NLR寡聚化Ⅱ:共聚焦显微镜和免疫荧光法检测ASC斑点形成,M. Beilharz等,《分子生物学方法》,2016年,第1417卷,145页
3. 炎症小体激活的无细胞实验,Y. Jamilloux & F. Martinon,《分子生物学方法》,2016年,第1417卷,207页
4. 流式细胞术检测人外周血中ASC斑点——炎症小体激活的读数指标,N. Wittmann等,《细胞》,2021年,第10卷,2880页
5. 炎症小体激活后人原代角质形成细胞中的ASC斑点形成,N. Smatlik等,《氧化医学与细胞长寿》,2021年,7914829
●Casper-1、Casper-2、Bally-1和Cryo-2相关实验方案
1. 炎症小体的检测,O. Gross,《分子生物学方法》,2012年,第844卷,199页
2. 活化半胱天冬酶-1的免疫印迹检测,C. Jakobs等,《分子生物学方法》,2013年,第1040卷,103页
3. 检测NLR寡聚化Ⅰ:体积排阻色谱、免疫共沉淀和交联法,S. Khare等,《分子生物学方法》,2016年,第1417卷,131页
4. 半胱天冬酶-1激活的检测,B. Guey & V. Petrilli,《分子生物学方法》,2016年,第1417卷,197页
5. 炎症小体激活的无细胞实验,Y. Jamilloux & F. Martinon,《分子生物学方法》,2016年,第1417卷,207页
产品名称 | 货号 | 规格 | 来源/同型 | 种属 | 应用 |
NOD样受体(NLRs) | - | - | - | - | - |
抗小鼠NAIP1/2/5单克隆抗体(Naipa-1) | AG-20B-0045 | 100μg | 小鼠IgG2b κ | 小鼠 | WB |
抗人NLRP1/NALP1多克隆抗体(AL176) | AG-25B-0005 | 100μg | 兔 | 人 | WB |
抗NLRP3/NALP3单克隆抗体(Cryo-2) | AG-20B-0014 | 100μg | 小鼠IgG2b | 人、小鼠 | ICC、IHC、IP、WB |
抗小鼠NLRP3/NALP3单克隆抗体(Cryo-1) | AG-20B-0006 | 100μg | 小鼠IgG2b | 小鼠 | WB |
抗人NLRP6/NALP6单克隆抗体(Clint-1) | AG-20B-0046 | 100μg | 小鼠IgG1 κ | 人 | WB |
RIG样解旋酶(RLHs)——抗病毒信号通路 | - | - | - | - | - |
抗RIG-I单克隆抗体(Alme-1) | AG-20B-0009 | 100μg | 小鼠IgG1 | 人、小鼠 | IHC、IP、WB |
抗RIG-I单克隆抗体(Alme-1,生物素标记) | AG-20B-0009B | 100μg | 小鼠IgG1 | 人、小鼠 | IHC、IP、WB |
抗人Cardif单克隆抗体(Adri-1) | AG-20B-0004 | 100μg | 小鼠IgG2b | 人 | ICC、IHC、IP、WB |
抗人MDA5单克隆抗体(Hely-1) | AG-20B-0013 | 100μg | 小鼠IgG1 | 人 | ELISA、IP、WB |
抗丙型肝炎病毒NS3单克隆抗体(1B6) | AG-20B-0001 | 100μg | 小鼠IgG1 | 丙型肝炎病毒 | ICC、WB |
抗丙型肝炎病毒NS5B单克隆抗体(5B-3B1) | AG-20B-0002 | 100μg | 小鼠IgG2b | 丙型肝炎病毒 | WB |
抗丙型肝炎病毒NS5B封闭性单克隆抗体(5B-12B7) | AG-20B-0003 | 100μg | 小鼠IgG2a | 丙型肝炎病毒 | ICC、IP、功能学应用(封闭) |
细胞质DNA传感器 | - | - | - | - | - |
抗人AIM2单克隆抗体(3B10) | AG-20B-0040 | 100μg | 小鼠IgG1 | 人 | ICC、WB |
细胞质细菌传感器 | - | - | - | - | - |
抗人Pyrin多克隆抗体(AL196) | AG-25B-0020 | 100μg | 兔 | 人 | IP、WB |
细胞质病原体相关分子模式传感器 | - | - | - | - | - |
抗半胱天冬酶-4/11(p20)单克隆抗体(Flamy-1) | AG-20B-0060 | 100μg | 小鼠IgG2b κ | 人、小鼠 | IP、WB |
抗半胱天冬酶-4/11(p20)单克隆抗体(Flamy-1,生物素标记) | AG-20B-0060B | 100μg | 小鼠IgG2b κ | 人、小鼠 | IP、WB |
七、炎症小体激活的定量检测——白细胞介素-1β(IL-1β)
货号AG-45B-0021-KI01,规格96孔
同型 | 小鼠IgG |
特异性 | 检测人IL-1β |
种属反应性 | 人 |
灵敏度 | 0.7皮克/毫升 |
检测范围 | 1.5625皮克/毫升~100皮克/毫升 |
检测类型 | 比色法/夹心ELISA |
样本类型 | 细胞培养上清液、血清、血浆 |
在病原体相关分子模式(PAMPs)或损伤相关分子模式(DAMPs)等预激活信号作用下,IL-1β以无活性的35kDa前体形式产生;在组织损伤或疾病状态下,炎症小体激活后该前体被切割为17kDa的活性形式。活性IL-1β在启动和扩散无菌性炎症中发挥已知作用,包括募集巨噬细胞、激活促炎性细胞因子白细胞介素-6(IL-6)以及调控趋化因子的表达。
我司新品人IL-1β ELISA试剂盒可高灵敏度、高特异性地检测生物体液中的全长和切割型人IL-1β。
抗小鼠IL-1α(p18)单克隆抗体(Teo-1),货号AG-20B-0064-C100,规格100微克
• 同型:小鼠IgG
• 应用:WB(1微克/毫升)
• 特异性:识别小鼠IL-1α的切割型p18片段和全长片段

实验图:采用抗小鼠IL-1α(p18)单克隆抗体(Teo-1,货号AG-20B-0064),通过免疫印迹检测到小鼠IL-1α(全长p30片段和切割型p18片段)。
实验方法:对经脂多糖(LPS)和多种炎症小体激活剂处理的骨髓源树突状细胞(BMDCs)的细胞提取物和上清液进行蛋白质免疫印迹,分析IL-1α。将细胞提取物和上清液经还原条件下的SDS-PAGE分离,转印至硝酸纤维素膜,与1微克/毫升的抗小鼠IL-1α(p18)单克隆抗体(Teo-1)孵育,加入辣根过氧化物酶(HRP)偶联的抗小鼠二抗后,采用化学发光检测系统显色。
泳道说明:1-脂多糖预激活的骨髓源树突状细胞裂解液;2-脂多糖+三磷酸腺苷(ATP)处理的骨髓源树突状细胞上清液;3-脂多糖+尼日利亚菌素处理的骨髓源树突状细胞上清液;4-脂多糖+尿酸单钠结晶处理的骨髓源树突状细胞上清液。
NLRP3是炎症小体复合物的核心组分,在炎症调控中发挥关键作用。NLRP3可响应多种刺激,从而抵御多种病毒和细菌感染,如腺病毒、流感病毒、冠状病毒、金黄色葡萄球菌、鼠伤寒沙门氏菌、单核细胞增生李斯特菌和分枝杆菌。
这些病原体相关分子模式(PAMPs)以及部分非病原性刺激(损伤相关分子模式DAMPs)可通过预激活和激活/触发两步过程增强NLRP3炎症小体的激活。
预激活至少发挥两大作用:
1. 上调炎症小体组分NLRP3、半胱天冬酶-1和IL-1β前体的表达:病原体相关分子模式(PAMPs)或损伤相关分子模式(DAMPs)与模式识别受体(PRRs,如Toll样受体TLRs、核苷酸结合寡聚化结构域蛋白2 NOD2)结合,或肿瘤坏死因子(TNF)、IL-1β等细胞因子激活核因子-κB(NF-κB)并启动基因转录,均可诱导上述组分的转录上调;
2. 诱导NLRP3的翻译后修饰(PTMs):该修饰使NLRP3稳定在自身抑制的无活性但可响应信号的状态。目前已发现NLRP3的多种翻译后修饰,包括泛素化、磷酸化和小泛素化修饰(SUMO化)。
与其他模式识别受体不同,NLRP3可被细菌、病毒、真菌感染引发的多种不相关刺激激活,也可在内源性DAMPs介导的无菌性炎症中,或暴露于环境刺激物后被激活。这些激活剂的共同特征是均能诱导细胞应激,并被NLRP3感知。
NLRP3的激活涉及多种上游信号(多数信号并非互斥),包括钾离子(K⁺)/氯离子(Cl⁻)外流、钙离子(Ca²⁺)内流、溶酶体破裂、线粒体功能障碍、代谢变化和反式高尔基体解体。
当病原体相关分子模式(PAMPs)存在或损伤相关分子模式(DAMPs,如ATP、尿酸结晶、活性氧ROS)累积时,NLRP3炎症小体复合物组装,进而启动其实际激活过程。复合物形成后激活半胱天冬酶-1,将IL-1β前体和IL-18前体切割为活性形式,促使这些细胞因子释放并启动免疫反应。
此外,翻译后修饰(PTMs)是NLRP3激活的关键调控因子,可影响蛋白质的活性、降解、定位、结构及与其他蛋白的相互作用等多个方面。
1. NLRP3炎症小体激活调控机制的进展,S. Paik等,《细胞与分子免疫学杂志》,2021年,第18卷,1141页
2. 炎症衰老和年龄相关疾病中NLRP3炎症小体的预激活机制,A. Gritsenko等,《细胞因子与生长因子评论》,2020年,第55卷,15页
3. NLRP3炎症小体的预激活:一层套一层的未解之谜,C.M. McKee & R.C. Coll,《白细胞生物学杂志》,2020年,第108卷,937页
NLRP3炎症小体最主要的功能是加工并激活IL-1β前体,而多数细胞并不表达IL-1β前体,因此需先诱导其表达。TLR配体、肿瘤坏死因子(TNF)等多种刺激均可诱导IL-1β前体的合成。
脂多糖(LPS) 通过TLR4介导的信号通路发挥作用,因其高效性和易获取性,始终是诱导IL-1β前体产生的配体;同时,LPS刺激还能触发NLRP3的多种翻译后修饰(如泛素化),这是NLRP3预激活过程的关键步骤。
1. 佛波醇12-肉豆蔻酸13-乙酸酯(PMA),货号AG-CN2-0010
2. 可溶性人肿瘤坏死因子-α(重组),货号AG-40B-0006
3. 多聚体人肿瘤坏死因子-α(重组),货号AG-40B-0019
4. 多聚体小鼠肿瘤坏死因子-α(重组),货号AG-40B-0021
5. 脂多糖(LPS)
1. 无菌性炎症疾病中的炎症小体预激活,M.N. Patel等,《分子医学趋势》,2017年,第23卷,165页
2. NLRP3激活的关键:预激活和溶酶体损伤,V. Hornung & E. Latz,《欧洲免疫学杂志》,2010年,第40卷,620页
3. 炎症小体,K. Schröder & J. Tschopp,《细胞》,2010年,第140卷,821页
完整产品列表详见我司《固有免疫研究手册》。
探索我司多款即用型LPS溶液,专为炎症小体预激活设计。无需自行溶解LPS,选择AdipoGen生命科学的均一即用型LPS溶液,直接使用即可。
九、翻译后修饰(PTMs)和蛋白结合对NLRP3炎症小体的调控
NLRP3是一种细胞质模式识别受体,在炎症调控中起核心作用。其预激活和激活受多种翻译后修饰(PTMs) 调控(如下文),本部分仅为概述,并非涵盖全部修饰类型。
磷酸化调控NLRP3的活性,是预激活过程的关键步骤。NLRP3的磷酸化位点及作用如下:
• 丝氨酸198(小鼠为丝氨酸194):由c-Jun N端激酶1(JNK1)磷酸化,促进NLRP3的去泛素化和寡聚化;
• PYD-NACHT碱性接头区的4个酪氨酸残基(Tyr132、Tyr136、Tyr145、Tyr164):由布鲁顿酪氨酸激酶(BTK)磷酸化,中和该区域的正电荷,使NLRP3从完整的反式高尔基体网络(TGN)转移至分散的反式高尔基体网络,促进NLRP3炎症小体组装;
• 丝氨酸5:由AKT或BTK磷酸化,抑制Asc与NLRP3的结合及炎症小体激活,该过程可被磷酸酶PP2A逆转;
• 人丝氨酸295(小鼠丝氨酸293):由蛋白激酶D(PKD)磷酸化,使NLRP3从高尔基体释放并激活;由蛋白激酶A(PKA)磷酸化,抑制NLRP3的ATP酶活性。
此外,非受体型蛋白酪氨酸磷酸酶22(PTPN22)可与NLRP3相互作用,并使其酪氨酸861位点去磷酸化(该位点的磷酸化激酶尚未明确)。
NLRP3的泛素化和去泛素化调控其稳定性和活性:TLR4和MyD88介导的信号通路可触发NLRP3的去泛素化,进而诱导炎症小体激活;去泛素化酶(DUBs)在NLRP3调控中起重要作用,其小分子抑制剂可阻断NLRP3的激活。
具体调控机制:
• BRCC3介导NLRP3富亮氨酸重复序列(LRR)结构域的去泛素化,是NLRP3寡聚化的必要条件;
• FBXL2使NLRP3的LRR结构域泛素化,促进其经蛋白酶体降解;
• ARIH2与NLRP3的NACHT结构域结合,诱导其K48位连接的泛素化,进而通过蛋白酶体介导降解;
• E3泛素连接酶MARCH7使NLRP3的LRR结构域发生K48位连接的泛素化,通过自噬途径诱导其降解。
NLRP3的SUMO化调控其稳定性和功能:
• 小泛素样修饰物(SUMO)E3连接酶MUL1/MAPL可介导NLRP3的SUMO化;NLRP3激活信号可诱导SENP6和SENP7介导其去SUMO化;
• SUMO1介导的SUMO化具有激活作用,是NLRP3激活的必要条件;SENP3介导的去SUMO化则会抑制NLRP3激活;
• 重要发现:LPS预激活对NLRP3的SUMO化无明显影响。
还包括乙酰化(激活作用,促进NLRP3聚集并与ASC结合)和亚硝基化(NLRP3的负调控因子)。
总体而言,NLRP3、Asc和半胱天冬酶-1的翻译后修饰在调控NLRP3活性及其炎症调控功能中发挥关键作用。除转录和翻译后调控机制外,多种蛋白结合伴侣也可正向或负向调控NLRP3的预激活和激活,包括:
• NIMA相关激酶7(NEK7,丝氨酸-苏氨酸激酶):NLRP3炎症小体组装和激活的关键组分;
• 仅含PYD结构域蛋白(POPs):细胞质中的小型诱饵蛋白,调控炎症小体激活(仅在人细胞中存在);
• 仅含CARD结构域蛋白(COPs):调控机制尚不明确(仅在人细胞中存在)。
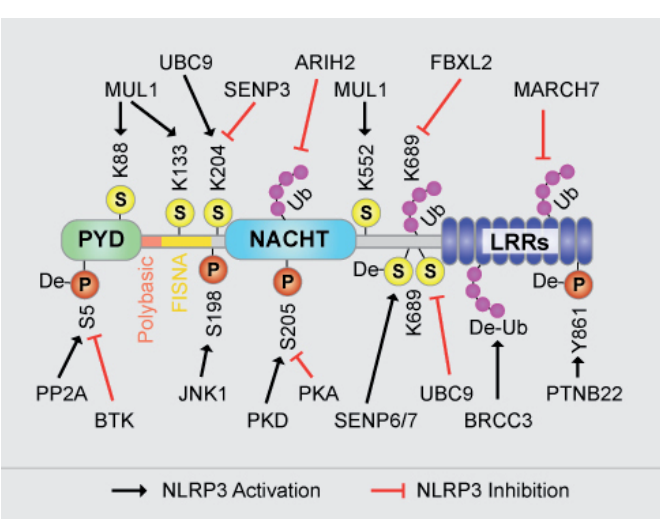
实验图:人NLRP3的分子结构与翻译后修饰(NLRP3激活/抑制相关)。
1. 翻译后修饰在NLRP3炎症小体激活调控中的作用,J. Xia等,《国际分子科学杂志》,2023年,第24卷,6126页
2. 翻译后修饰对NLRP3炎症小体的调控,S. Zangiabadi & A.A. Abdul-Sater,《免疫学杂志》,2022年,第208卷,286页
3. 塑造炎症小体:磷酸化是炎症小体信号通路的关键开关,C.M. McKee等,《生物化学会汇刊》,2021年,第49卷,2495页
NLRP3是开发新型抗炎疗法的潜力的靶点,NLRP3小分子直接抑制剂已显示出良好的应用前景。此外,参与NLRP3预激活(转录和翻译后水平)的多种其他蛋白,也可作为靶点以抑制NLRP3介导的炎症。
产品名称 | 靶点 | 货号 |
SP 600125 | JNK抑制剂 | AG-CR1-3549 |
CRT0066101 盐酸盐 | PDK抑制剂 | AG-CR1-3550 |
冈田酸 | PP2A抑制剂 | AG-CN2-0056 |
WP1130 | 去泛素化酶(DUB)抑制剂 | AG-CR1-3551 |
β-AP15 | 去泛素化酶(DUB)抑制剂 | AG-CR1-3552 |
货号:AG-CR1-3950(结晶型,2毫克/2×2毫克/5毫克/25毫克)、AG-CR1-3951(即用型溶液,10毫克/250毫克/1克/5克),经生物活性验证! 高效NLRP3炎症小体激活剂。
相关文献:痛风相关尿酸结晶激活NALP3炎症小体,F. Martinon等,《自然》,2006年,第440卷,237页。
●尼日利亚菌素钠([Nigericin.Na](Nigericin.Na))
货号AG-CN2-0020,高效NLRP3炎症小体激活剂。
相关文献:冷吡啉响应毒素和ATP激活炎症小体,S. Mariathasan等,《自然》,2006年,第440卷,228页。
货号AG-CN2-0489,通过使己糖激酶与线粒体解离,成为NLRP3炎症小体的新型激活剂。
相关文献:己糖激酶是检测细菌肽聚糖的固有免疫受体,A.J. Wolf等,《细胞》,2016年,第166卷,624页。
产品名称 | 货号/规格 | 作用特点 | 相关文献 |
紫菀内酯(Arglabin) | AG-CN2-0458,1mg/5mg/10mg/50mg | NLRP3炎症小体抑制剂 | 紫菀内酯的抗炎和抗动脉粥样硬化作用(高脂饮食ApoE2 Ki小鼠模型),A. Abderrazak等,《循环》,2015年,第131卷,1061页 |
BAY 11-7082 | AG-CR1-0013,1mg/5mg/10mg/50mg | 抑制NLRP3炎症小体,降低其ATP酶活性 | 抗炎化合物小白菊内酯和BAY 11-7082是炎症小体的直接抑制剂,C Juliana等,《生物化学杂志》,2010年,第285卷,9792页 |
达潘苏特rile(Dapansutrile) | AG-CR1-3535,10mg/50mg/250mg,可批量供应 | 高效、高选择性、口服有效的NLRP3抑制剂,直接结合NLRP3 NACHT结构域的ATP结合基序 | - |
MCC950钠 | AG-CR1-3615,1mg/5mg/10mg,可批量供应 | 高效、高选择性NLRP3炎症小体抑制剂 | 1. NLRP3炎症小体小分子抑制剂用于治疗炎症性疾病,R.C. Coll等,《自然医学》,2015年,第21卷,248页;2. NLRP3抑制剂OLT1177抑制小鼠急性关节炎模型的关节炎症,C Marchetti等,《关节炎研究与治疗》,2018年,第20卷,169页 |
前列腺素E2 | AG-CR1-3613,1g/5g/10g | NLRP3炎症小体抑制剂 | 前列腺素E2通过EP4受体和细胞内环磷酸腺苷抑制人巨噬细胞的NLRP3炎症小体激活,M. Sokolowska等,《免疫学杂志》,2015年,第194卷,5472页 |
格列本脲(USP级) | AG-CL1-0001,1mg/5mg/25mg/100mg | 抑制NLRP3的ATP酶活性(NLRP3-Asc炎症小体复合物组装的必要条件) | NLRP3炎症小体小分子抑制剂用于治疗炎症性疾病,R.C Coll等,《自然医学》,2015年,第21卷,248页 |
(S)-3-羟基丁酸/3-羟基丁酸/(R)-3-羟基丁酸 | AG-CR1-3617,25mg/100mg | NLRP3炎症小体抑制剂,抑制钾离子外流,进而减少Asc寡聚化和斑点形成 | 酮代谢物β-羟基丁酸阻断NLRP3炎症小体介导的炎症性疾病,Y.H. Youm等,《自然医学》,2015年,第21卷,263页 |
小白菊内酯(Parthenolide) | AG-CN2-0455,10mg/50mg/250mg | 抑制NLRP3炎症小体,降低其ATP酶活性 | 抗炎化合物小白菊内酯和BAY 11-7082是炎症小体的直接抑制剂,C Juliana等,《生物化学杂志》,2010年,第285卷,9792页 |
异甘草素(Isoliquiritigenin) | AG-CN2-0459,25mg/100mg | 抑制NLRP3激活的Asc寡聚化,阻断预激活和激活步骤 | 异甘草素是NLRP3炎症小体的高效抑制剂,可抑制饮食诱导的脂肪组织炎症,H. Honda等,《白细胞生物学杂志》,2014年,第96卷,1087页 |
K777[K11777] | AG-CR1-0158 | 广谱组织蛋白酶抑制剂,可用于抑制炎症小体 | 多种组织蛋白酶在NLRP3依赖的IL-1β激活过程中,促进颗粒诱导的非炎症小体依赖性细胞死亡,GM. Orlowski等,《白细胞生物学杂志》,2017年,第102卷,7页 |
十三、 炎症小体及其治疗意义
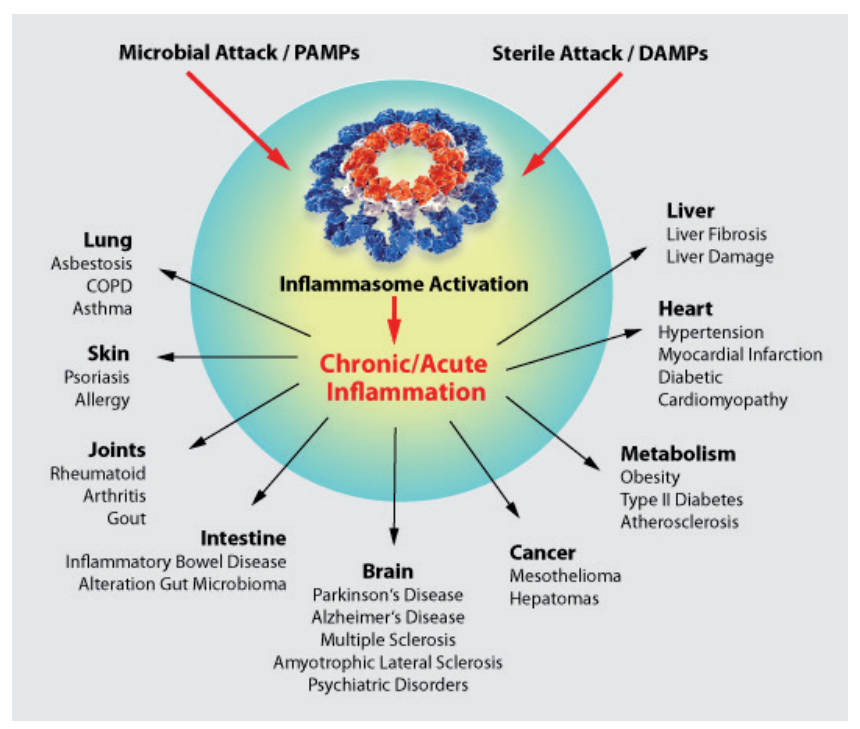
炎症小体的异常激活与慢性炎症密切相关,是多种疾病发生发展的诱因——因其在调控免疫反应和促炎性细胞因子产生中发挥关键作用。靶向炎症小体已成为治疗多种疾病的潜在策略,包括:
• 炎症性疾病(如关节炎、痛风、炎症性肠病);
• 自身免疫性疾病(如红斑狼疮、多发性硬化症);
• 代谢性疾病(如2型糖尿病、肥胖、心血管疾病);
• 癌症、神经退行性疾病。
近期研究还表明,NLRP3炎症小体与病毒感染、败血症等其他疾病相关。在上述疾病的动物模型中,抑制炎症小体激活或靶向炎症小体组分可有效减轻炎症。总体而言,靶向炎症小体具有巨大的治疗潜力,是开发新型疗法的重要方向。
炎症小体激活相关疾病累及器官/系统:肺(石棉肺、哮喘、慢性阻塞性肺疾病COPD)、皮肤(银屑病、过敏、急/慢性炎症)、关节(类风湿关节炎)、代谢系统(肥胖、2型糖尿病)、肠道(炎症性肠病、肠道微生物群紊乱、痛风)、心脏(高血压、心肌梗死、糖尿病心肌病)、肝脏(肝损伤、肝纤维化)、大脑(帕金森病、阿尔茨海默病、多发性硬化症、精神疾病)、其他(癌症、间皮瘤、肝癌、动脉粥样硬化)。
1. NLRP3炎症小体通路抑制剂——炎症性疾病的潜在治疗候选药物,X. Zhang等,《国际分子医学杂志》,2023年,第51卷,35页
2. NLRP3炎症小体的药理学抑制:结构、分子激活及抑制剂-NLRP3相互作用,Q. Ma,《药理学评论》,2023年,第75卷,487页
3. 聚焦NLRP3炎症小体在疾病中的作用,R. Fusco等,《国际分子科学杂志》,2020年,第21卷,4223页
免疫代谢是研究免疫细胞内的代谢过程和通路如何影响其功能的学科。免疫细胞在炎症反应中被激活时,会发生显著的代谢变化以满足其增加的能量需求,主要表现为从氧化磷酸化向糖酵解转换——糖酵解产能更快但效率更低。
炎症小体的活性受细胞内代谢通路变化的严格调控,近期研究表明,调控免疫代谢可调节免疫反应、降低炎症小体活性并减轻炎症。例如,促进免疫细胞的脂肪酸代谢或阻断其糖酵解,可诱导抗炎反应。
1. NLRP3炎症小体:代谢信号的调控作用,A. Olona等,《免疫学趋势》,2022年,第43卷,978页
2. 靶向免疫代谢作为抗炎策略,E.M. Palsson-McDermott & L. O’Neill,《细胞研究》,2020年,第30卷,300页
产品名称 | 靶点 | 货号 |
2-脱氧-D-葡萄糖 | 己糖激酶抑制剂 | AG-CR1-3681 |
富马酸二甲酯 | Nrf2激活剂 | AG-CR1-3701 |
庚二酸 | 甘油醛-3-磷酸脱氢酶(GADPH)抑制剂 | AG-CN2-0118 |
盐酸二甲双胍 | 活性氧(ROS)抑制剂 | AG-CR1-3689 |
雷帕霉素 | 哺乳动物雷帕霉素靶蛋白(mTOR)抑制剂 | AG-CN2-0025 |
TEPP-46 | 丙酮酸激酶M2(PKM2)激活剂 | AG-CR1-3687 |
微管是细胞骨架的重要组分,除参与细胞分裂、迁移和形态维持等基本功能外,在固有免疫中也发挥关键作用。炎症小体由模式识别受体、衔接蛋白Asc和半胱天冬酶-1组装而成,可响应病原体相关分子模式(PAMPs)或损伤相关分子模式(DAMPs),加工IL-1β和IL-18。
1. 预激活后:NLRP3表达并结合于内质网和反式高尔基体网络(TGN)的胞内膜,组装为寡聚化双环笼状结构(PYD结构域包埋在内),此为无活性状态;
2. 激活后:NLRP3激活剂诱导微管的聚合和乙酰化,反式高尔基体网络囊泡与NLRP3分散,并被转运至微管组织中心(MTOC),与NEK7结合形成预激活炎症小体复合物(无Asc和半胱天冬酶-1前体);
3. 无活性的NLRP3寡聚笼状结构通过结合乙酰化α-微管蛋白的HDAC6-动力蛋白复合物,沿微管从反式高尔基体网络转运至微管组织中心;
4. 反式高尔基体网络囊泡通过微管释放,使NLRP3重新定位至线粒体附近的细胞质,线粒体上的Asc和半胱天冬酶-1前体与NLRP3近距离接触并相互作用,形成活性NLRP3炎症小体复合物。
关键发现:α-微管蛋白的乙酰化是NLRP3激活的核心步骤,其机制为NLRP3激活引发线粒体功能障碍,进而导致乙酰化α-微管蛋白累积。
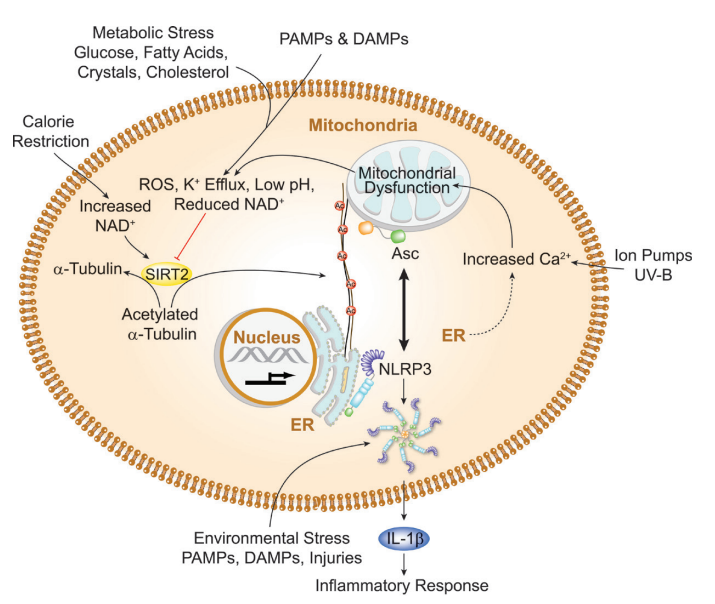
实验图:乙酰化α-微管蛋白的累积通过促进线粒体上的Asc与内质网上的NLRP3相互作用,推动炎症小体的组装和激活。
1. 小鼠全长NLRP3结构揭示的NLRP3笼状结构调控通路激活,L. Andreeva等,《细胞》,2021年,第184卷,6299页
2. 笼状NLRP3调控炎症小体活性,K. Schroder & R.C Coll,《细胞》,2021年,第184卷,6224页
产品名称 | 货号 | 规格 | 来源 | 应用 |
抗乙酰化α-微管蛋白单克隆抗体(TEU318) | AG-20B-0068 | 100μg | 小鼠IgG1 | ICC、WB |
抗糖基化微管蛋白多克隆抗体(Gly-pep1) | AG-25B-0034 | 100μg | 兔 | ICC、IP、WB |
抗GTP化微管蛋白重组单克隆抗体(MB11) | AG-27B-0009 | 100μg | 人IgG2 λ | ICC |
抗β-微管蛋白(β-单谷氨酸化)多克隆抗体(IN115) | AG-25B-0039 | 50μg | 兔 | ICC、IHC、IP、WB |
抗多聚谷氨酸化修饰单克隆抗体(GT335) | AG-20B-0020 | 100μg | 小鼠IgG1k | 电镜(EM)、ICC、IP、WB |
抗多聚谷氨酸化修饰单克隆抗体(GT335,生物素标记) | AG-20B-0020B | 100μg | 小鼠IgG1k | ICC、IP、WB |
抗多聚谷氨酸链(多聚E)多克隆抗体(IN105) | AG-25B-0030 | 50μg | 兔 | ICC、WB |
1. 秋水仙碱(Colchicine),货号AG-CN2-0048,规格500mg/1g:微管抑制剂,抑制乙酰化α-微管蛋白介导的线粒体转运,进而阻断线粒体上的Asc与内质网上的NLRP3的相互作用(相关文献:微管驱动的线粒体空间排布促进NLRP3炎症小体激活,T. Misawa等,《自然免疫学》,2013年,第14卷,454页);
2. 动力蛋白抑制剂:Dynasore(AG-CR1-0045);
3. F-肌动蛋白稳定剂:Jasplakinolide(AG-CN2-0037);
4. F-肌动蛋白解聚剂:Latrunculin A(AG-CN2-0027)、Latrunculin B(AG-CN2-0031)、细胞松弛素B(AG-CN2-0504)、葫芦素E(AG-CN2-0474);
5. F-肌动蛋白抑制剂:Swinholide A(AG-CN2-0035);
6. 微管抑制剂:秋水仙胺(AG-CR1-3567)、伊里诺醌(AG-CN2-0038)、诺考达唑(AG-CR1-0019)、鬼臼毒素(AG-CN2-0049)、拟海松酸B(AG-CN2-0083);
7. 微管稳定剂:紫杉醇(AG-CN2-0045);
8. 微管抑制剂:帚曲霉素A(AG-CN2-0515)。
相关文献:微管驱动的线粒体空间排布促进NLRP3炎症小体的激活,T. Misawa等,《自然免疫学》,2013年,第14卷,454页
产品名称 | 作用靶点 | 货号 |
动力蛋白抑制剂(Dynasore) | 动力蛋白抑制剂 | AG-CR1-0045 |
Jasplakinolide | F-肌动蛋白稳定剂 | AG-CN2-0037 |
拉春库林A(Latrunculin A) | F-肌动蛋白解聚剂 | AG-CN2-0027 |
拉春库林B(Latrunculin B) | F-肌动蛋白解聚剂 | AG-CN2-0031 |
斯维内酯A(Swinholide A) | F-肌动蛋白抑制剂 | AG-CN2-0035 |
细胞松弛素B(Cytochalasin B) | 肌动蛋白解聚剂 | AG-CN2-0504 |
葫芦素E(Cucurbitacin E) | 肌动蛋白解聚剂 | AG-CN2-0474 |
秋水仙胺(Colcemid) | 微管抑制剂 | AG-CR1-3567 |
伊里诺醌(Ilimaquinone) | 微管抑制剂 | AG-CN2-0038 |
诺考达唑(Nocodazole) | 微管抑制剂 | AG-CR1-0019 |
紫杉醇(Paclitaxel) | 微管稳定剂 | AG-CN2-0045 |
磷霉素A(Phomopsin A) | 微管抑制剂 | AG-CN2-0515 |
鬼臼毒素(Podophyllotoxin) | 微管抑制剂 | AG-CN2-0049 |
伪绵马酸B(Pseudolaric acid B) | 微管抑制剂 | AG-CN2-0083 |
经典炎症小体 | 非经典炎症小体 |
关键组分:吡喃蛋白、NLRP1b、NLRP3、NLRC4、AIM2、半胱天冬酶-1前体 | 关键组分:半胱天冬酶-11/4/5前体、脂多糖(LPS) |
激活过程:传感器蛋白识别刺激后,与衔接蛋白Asc、半胱天冬酶-1前体组装形成寡聚化活性炎症小体复合物 | 激活过程:半胱天冬酶-11/4/5前体识别LPS后发生寡聚化并激活 |
下游效应:半胱天冬酶-1激活,切割IL-1β前体(p30)产生活性IL-1β,切割气膜蛋白D(GSDMD)释放N端片段 | 下游效应:激活的半胱天冬酶-11/4/5切割气膜蛋白D(GSDMD)释放N端片段 |
最终结果:IL-1β分泌至细胞外,气膜蛋白D N端片段在细胞膜形成孔道,引发焦亡和炎症反应 | 最终结果:气膜蛋白D N端片段在细胞膜形成孔道,引发焦亡和炎症反应 |
抗小鼠气膜蛋白D(C端)多克隆抗体(IN110)
货号:AG-25B-0036,规格:100微克
• 抗体来源:豚鼠
• 免疫原:重组小鼠气膜蛋白D(C端)
• 适用实验:酶联免疫吸附测定(ELISA)、蛋白质印迹(WB)
• 特异性:识别小鼠气膜蛋白D的全长及切割型C端结构域,与人气膜蛋白D无交叉反应
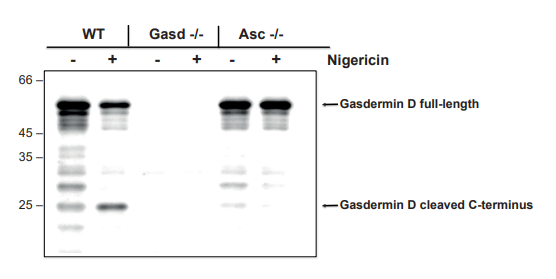
图:采用抗小鼠气膜蛋白D多克隆抗体(IN110,货号AG-25B-0036),通过免疫印迹法检测到小鼠气膜蛋白D(全长及切割型p22片段)。
实验方法:用50纳克/毫升脂多糖(LPS,货号AG-CU1-0001)处理野生型(WT)、气膜蛋白D基因敲除(Gasd -/-)或Asc基因敲除(Asc -/-)小鼠的骨髓来源巨噬细胞(BMDMs)3小时,再用5微摩尔尼日利亚菌素(货号AG-CN2-0020)处理2.5小时(或不处理),提取细胞提取物通过蛋白质印迹法分析气膜蛋白D。将细胞提取物经还原条件下的SDS-PAGE分离,转印至硝酸纤维素膜,与0.5微克/毫升的抗小鼠气膜蛋白D多克隆抗体(IN110)孵育;加入1:5000稀释的辣根过氧化物酶(HRP)偶联抗豚鼠二抗后,通过化学发光检测系统显色。
图片来源:德国弗莱堡大学医学中心Olaf Gross教授提供
焦亡是一种炎症性程序性细胞死亡,由病原体或宿主来源的细胞质扰动触发。炎症小体传感器激活后,会激活半胱天冬酶-1及其他炎性半胱天冬酶,这些酶切割气膜蛋白D和IL-1β/IL-18前体,最终引发焦亡和成熟细胞因子分泌。
焦亡以细胞死亡为代价,破坏胞内病原体的生存环境并释放胞内成分,诱导邻近细胞产生促炎症反应。IL-1β是强效的促炎症调控因子,可募集中性粒细胞、激活巨噬细胞并促进T细胞增殖。因此,焦亡和细胞因子分泌是炎症小体信号通路下游的两大核心机制,它们维持机体稳态、驱动固有免疫反应并塑造适应性免疫。
气膜蛋白D(GSDMD)是焦亡的核心介导因子,包含功能性N端结构域和抑制性C端结构域。半胱天冬酶-1/11在气膜蛋白D两个结构域之间的连接区(人Asp275、小鼠Asp276)切割后,释放的N端片段发生寡聚化,在宿主细胞膜形成孔道,最终导致细胞焦亡。此外,细胞表面死亡受体连接和寡聚化激活的半胱天冬酶-8,也可触发气膜蛋白D依赖的焦亡。
1. 炎症小体信号通路下游焦亡与IL-1β分泌的解偶联,Y. Li、Q. Jiang,《免疫学前沿》,2023年,第14卷,1128358页
2. 焦亡的分子机制,J. Marisa等,《分子生物学方法》,2023年,第2641卷,1页
3. 气膜蛋白的“失控":气膜蛋白家族在调控细胞稳态中的新作用,C.G. Weindel等,《细胞生物学趋势》,2023年(在线优先出版)
4. 焦亡:一把两刃剑——在炎症性疾病和癌症中的致病作用与治疗潜力,Z. Liu等,《生命科学》,2023年,第318卷,121498页
FACS:流式细胞术;FUNC:功能实验;ICC:免疫细胞化学;IHC:免疫组化;IP:免疫沉淀;WB:蛋白质印迹;PF:无防腐剂;Hu:人;Ms:小鼠;Rt:大鼠;Rb:兔;Prm:灵长类
气膜蛋白D N端片段在细胞膜形成孔道后,其C端片段的功能和去向仍不明确。本公司的小鼠气膜蛋白D ELISA试剂盒(货号AG-45B-0011)可检测气膜蛋白D的C端片段及全长蛋白,在焦亡细胞的上清液中可检测到信号,表明C端片段会从细胞中释放——可能是由于孔道存在被动释放,也可能具有尚未明确的特定功能。
货号:AG-45B-0011,规格:1块96孔板
项目 | 说明 |
检测灵敏度 | 14皮克/毫升 |
检测范围 | 15.6-1000皮克/毫升 |
适用样本 | 细胞培养上清液、细胞裂解液 |
特异性 | 检测细胞培养上清液和细胞提取物中小鼠气膜蛋白D的全长及切割型C端片段,与人气膜蛋白D无交叉反应 |
验证实验:
1. 对转染脂多糖(LPS)的不同基因敲除小鼠品系的骨髓来源巨噬细胞(BMDMs)上清液进行检测(见图1),仅野生型(WT)和NLRP3基因敲除(NLRP3 KO)小鼠的上清液中检测到气膜蛋白D。
2. 对野生型和气膜蛋白D基因敲除(Gasd KO)小鼠的骨髓来源巨噬细胞(BMDMs)细胞提取物(用Triton X-100缓冲液裂解)进行检测(见图2),仅野生型小鼠的细胞提取物中检测到气膜蛋白D。
货号:AG-CR1-3698,规格:1毫克/5毫克
• 作用:气膜蛋白D N端片段(GSDMD-N)诱导焦亡的抑制剂,可保护巨噬细胞免受GSDMD-N的细胞毒性,或保护小鼠免受致死性感染
• 分子式:C₂₉H₄₀O₃
• 分子量:464.6
• CAS号:112648-68-7
相关文献:脂质过氧化驱动气膜蛋白D介导的焦亡在致死性混合菌脓毒症中的作用,R. Kang等,《细胞宿主与微生物》,2018年,第24卷,97页
货号:AG-CR1-3705,规格:5毫克/25毫克
• 作用:气膜蛋白D抑制剂,适用于小鼠研究,可直接结合气膜蛋白D,抑制其N端片段寡聚化,进而阻断孔道形成和焦亡
• 分子式:C₁₈H₁₅N₅O₂S
• 分子量:461.5
• CAS号:1360614-48-7
相关文献:化学阻断焦亡孔形成蛋白气膜蛋白D可抑制炎症性细胞死亡和脓毒症,J.K. Rathkey等,《科学免疫学》,2018年,第3卷,eaat2738页
半胱天冬酶-3/-7切割气膜蛋白E(GSDME)后,其N端焦亡诱导结构域(GSDME-NT)从自身抑制的C端调控结构域中释放,进而触发细胞膜孔道形成和焦亡。人类气膜蛋白E(GSDME)突变与遗传性非综合征性耳聋的发生相关。焦亡异常与多种人类疾病相关,包括感染、自身炎症性疾病、神经退行性疾病和癌症。
货号:AG-45B-0024,规格:1块96孔板
项目 | 说明 |
检测灵敏度 | 50皮克/毫升 |
检测范围 | 0.625-4纳克/毫升 |
适用样本 | 细胞培养上清液、血浆、血清 |
特异性 | 检测人气膜蛋白E的C端结构域及全长蛋白;气膜蛋白E切割和孔道形成后,其C端片段释放到细胞外,可在血清/血浆中检测到 |
Toll样受体5(TLR5)可识别革兰氏阳性菌和革兰氏阴性菌的鞭毛蛋白。该受体激活后,通过衔接蛋白MyD88、TIRAP和TRIF介导的信号传导,刺激肿瘤坏死因子-α(TNF-α)等促炎症细胞因子的产生。
鞭毛蛋白是聚合形成细菌鞭毛丝的亚基蛋白,不仅可通过TLR5激活固有免疫系统,还能通过胞内NAIP5/NLRC4(IPAF)炎症小体蛋白激活免疫反应。鞭毛蛋白激活NLRC4炎症小体和TLR5,是机体对细菌感染启动固有免疫反应的重要机制,在炎症调控中起关键作用。NLRC4炎症小体调控异常与脓毒症、炎症性肠病和某些类型癌症的发生相关。
AdipoGen生命科学公司提供多种低内毒素、高纯度的鞭毛蛋白产品,包括通路特异性突变体:
• 重组鞭毛蛋白(NLRC4突变体)(货号AG-40B-0126):仅能被TLR5识别,无法被NLRC4识别
• 重组鞭毛蛋白(TLR5突变体)(货号AG-40B-0127):仅能被NLRC4识别,无法被TLR5识别
产品名称 | 货号 | 规格 |
天然鞭毛蛋白 | AG-40B-0095 | 100微克 |
高纯度天然鞭毛蛋白 | AG-40B-0025 | 10微克、3×10微克 |
重组鞭毛蛋白(带组氨酸标签) | AG-40B-0125 | 10微克、3×10微克 |
重组鞭毛蛋白(无标签,高活性) | AG-40B-0243 | 50微克 |
重组鞭毛蛋白(NLRC4突变体) | AG-40B-0126 | 10微克、3×10微克 |
重组鞭毛蛋白(TLR5突变体) | AG-40B-0127 | 10微克、3×10微克 |
货号:AG-CR1-3548,规格:10毫克/50毫克
• 体外实验表明,m-3M3FBS可诱导线粒体损伤,并激活角质形成细胞中的NLRP10(与Asc和半胱天冬酶-1结合的功能性炎症小体)
• NLRP10在肠上皮细胞中也可作为炎症小体发挥作用,保护肠道免受自身炎症损伤
相关文献:
1. 线粒体损伤激活NLRP10炎症小体,T. Prochnicki等,《自然免疫学》,2023年,第24卷,595页
2. 上皮细胞Nlrp10炎症小体介导对肠道自身炎症的保护作用,D. Zheng等,《自然免疫学》,2023年,第24卷,585页
AIM2炎症小体抑制剂:苏拉明钠(Suramin sodium)
货号:AG-CR1-3575V,规格:50毫克/250毫克/1克
• 苏拉明是双链DNA(dsDNA)诱导炎症的有效抑制剂,可抑制多种双链DNA结合蛋白,包括固有免疫通路中的cGAS/STING
• 新研究表明,苏拉明可可逆性抑制小鼠和人的AIM2炎症小体
相关文献:一种优先靶向AIM2炎症小体的DNA驱动炎症抑制剂的发现,J.P. Green等,《交叉科学》,2023年,第26卷,106758页
更多产品信息,请联系中国区域代理商:上海起发实验试剂有限公司
如果您对任意产品或其他品牌感兴趣,可通过“在线留言"功能留下您的需求
(注:本文内容基于品牌公开资料及行业常规信息整理,具体以品牌信息文档为准。)
电话
微信
